
المحتوى
إلكترونات التكافؤ هي إلكترونات الطبقة الخارجية التي يمكن أن تملأها الذرة. أنها مهمة ، لأنها عادة ما تشارك في التفاعلات الكيميائية. يمثل الجدول الدوري للعناصر مرجعًا عمليًا لتحديد عدد إلكترونات التكافؤ في الذرة بسرعة. ومع ذلك ، تجدر الإشارة إلى أن العديد من العناصر ، معظمها المعادن الانتقالية وحتى بعض المعادن ، قد يكون لها عدة حالات تكافؤ ، وهذا يتوقف على المركب المحدد.
الاتجاهات
-
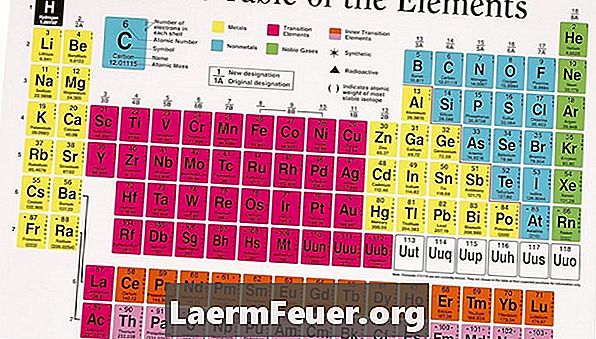
ابحث عن العنصر في الجدول الدوري. توجد في الجدول برقم ذري من اليسار إلى اليمين ، من أعلى إلى أسفل. يتوافق ترتيب العناصر في الخطوط مع الخصائص المشتركة بينها في عمود معين ، تحكمه بشكل كبير أوجه التشابه في ترتيب هذه الإلكترونات.
-
حدد العمود الذي يوجد به العنصر. تتم تسمية كل عمود برقم بالقرب من أعلى الصفحة. يتم ترقيم نظام الترقيم المقبول حاليًا بواسطة IUPAC من 1 إلى 8. سابقًا ، سمي IUPAC بالأعمدة 1A ، 2A ، 3A ، وهكذا. بينما يجب إعادة تعديل الجداول الدورية الجديدة إلى النظام الجديد ، يمكن للجداول القديمة استخدام التسمية السابقة.
-
حساب عدد الأعمدة من اليسار إلى اليمين ، مع تجاهل المعادن التي تمر بمرحلة انتقالية والعمود الأخير على اليمين. اكتبها كعدد الإلكترونات التكافلية. على سبيل المثال ، باستخدام نظام الترقيم السابق ، ما عليك سوى كتابة الأرقام الرومانية في العمود المسمى كأرقام الكترونية التكافؤ ، لعناصر في المجموعات IA و IIA و IIIA و IVA و VA و VIA و VIIA.
-
اكتب الصفر لعدد إلكترونات التكافؤ لعناصر المجموعة 18 (التي كانت تسمى سابقًا المجموعة VIIIA). تقدم هذه العناصر أقصى طبقة إلكترون مملوءة ، ولا تشارك بشكل عام في التفاعلات الكيميائية.
-
اكتب كلمة "يختلف" للعناصر الموجودة في الكتلة المعدنية الانتقالية في الجدول الدوري ، حيث أن ترتيب الإلكترونات في هذه العناصر يسمح لأولئك في الطبقة الأعمق بالمشاركة في التفاعلات الكيميائية. هذا يجعلهم يبدو أن لديهم التكافؤ الذي يتغير في ردود الفعل المختلفة. الحديد ، على سبيل المثال ، يتفاعل في بعض الأحيان باستخدام إلكترونين ، وثلاثة أخرى ، مما يعطيها تكافؤ واضح من اثنين أو ثلاثة.
ما تحتاجه
- الجدول الدوري للعناصر